Fernando Galán Galán
Profesor Titular de Medicina
Especialista en Medicina Interna
Experto en Miopatía Mitocondrial del Adulto
Fibromialgía y Síndrome de Fatiga crónica
BLOG
DISTINGUIENDO ENTRE LOS 14 TIPOS DEL SÍNDROME DE EHLERS DANLOS 2020. Principales Diagnósticos diferenciales y SOLAPAMIENTO (OVERLAPPING). 2ª parte
Principales Diagnósticos diferenciales
La osteogénesis imperfecta (OI) tipo I puede confundirse con algunos subtipos del síndrome de Ehlers-Danlos debido a la morbilidad significativa que sigue a traumatismos menores e hipermovilidad articular. Sin embargo, una combinación de sintomatología, además de las pruebas genéticas, puede distinguir los dos procesos de la enfermedad.
- Muchos pacientes con OI no deformante (OI tipo I) presentan esclerótica azul, sordera neurosensorial, huesos suturales o huesos wormianos y / o dentinogénesis imperfecta.
- Cabe mencionar que los pacientes con cualquier trastorno pueden presentar esclerótica azul. Además, pueden estar presentes mutaciones en los genes COL1A1 y COL1A2. Otros subtipos de OI no forman parte del diferencial.
El síndrome de Marfan (SMF)comparte muchas características similares con diferentes subtipos del síndrome de Ehlers-Danlos (específicamente el subtipo de hipermovilidad), sin embargo, el diagnóstico general del síndrome de Marfan puede separarse tanto clínica como genéticamente. Genéticamente, las mutaciones a menudo se identifican en el gen de la fibrilina-1. Clínicamente, cuando hay hiperlaxitud articular en un paciente con hábito marfanoide, ectopia lentis y / o patología de la raíz aórtica, se debe sospechar tanto de SED como de síndrome de Marfan. Sin embargo, es poco probable que la patología de la raíz aórtica, especialmente la ectasia, progrese en gravedad hasta la edad adulta, a diferencia de la progresión más común en el SMF. Además, la afectación del codo generalmente no se ve afectada y el hábito marfanoide es generalmente más obvio en el SMF con una relación entre el brazo y la altura superior a 1,05. Además, las pruebas genéticas de SMF pueden revelar una mutación en la proteína fibrilina 1, que no ocurre en la SED.
El síndrome de Loeys-Deitz (LDS)puede confundirse con el síndrome de Ehlers-Danlos debido a su patrón de herencia autosómico dominante y al diagnóstico precoz de patología aórtica, específicamente aneurismas. Sin embargo, existe una tríada clínica característica de LDS que ayuda al médico a guiar el diagnóstico.
- La tríada incluye úvula bífida / paladar hendido, hipertelorismo y aneurisma aórtico.
Más específicamente, los aneurismas descubiertos en un paciente con LDS se pueden detectar en todo el sistema arterial en lugar de agruparse alrededor de la raíz aórtica, como se observa más comúnmente en ciertos subtipos de SED.
- Mutación en los genes SMAD3;TGFB2;TGFBR1;TGFBR2
La cutis laxa puede confundirse con el síndrome de Ehlers-Danlos en el examen inicial. Sin embargo, es posible una distinción del examen tegumentario. Si bien muchos pacientes con SED poseen piel hiperextensible, su piel volverá casi de inmediato a su forma original después de una exploración adecuada. Se sabe que la piel de los pacientes con cutis laxa vuelve lentamente a su forma original debido a la distensión. La válvula cardíaca, la afectación vascular y la formación de hernias son tres características con una superposición significativa entre los dos procesos patológicos. . El análisis genético de pacientes con cutis laxa a menudo identificará mutaciones en el gen de la fibulina-5 (FBLN5) u otros genes: EFEMP2; LTBP4; ATP6V0A2; PYCR1; ELN
¿CÓMO LLEGAR AL DIAGNÓSTICO DEL SÍNDROME DE EHLERSDANLOS, INCLUYENDO LAS PRUEBAS GENÉTICAS?
¿Por qué se hacen las pruebas genéticas?
Para diagnosticar el SED, el equipo de atención médica realizará una revisión detallada de los síntomas del paciente, el historial médico de la familia y realizará exámenes físicos. Un médico que sospecha de SED puede ordenar una prueba genética para confirmar el diagnóstico.
Los resultados de la prueba genética pueden:
- Confirmar un diagnóstico de EDS
- Diferenciar entre los tipos de EDS
- Identificar a los portadores de EDS entre los miembros de la familia del paciente afectado.
Se pueden evaluar varios genes asociados con EDS en una prueba para determinar un cambio genético sospechado (mutación). Hay disponibles paneles con 18 -21 genes. Se utiliza una muestra de sangre para el análisis.
También se puede solicitar un examen genético de los miembros de la familia inmediata y extendida para determinar si otros están afectados.
- El panel que incluye los 21 genes prioritarios asociados con los diferentes subtipos de estos síndromes descritos hasta la fecha.
- Además, incluye 14 genes relacionados con enfermedades aórticas y otras enfermedades del tejido conectivo que predisponen a la dilatación y / o rotura de la aorta y otras arterias.
Este estudio permite analizar tanto variantes puntuales, como grandes duplicaciones y deleciones (variaciones en el número de copias, CNV) que pueden ser causantes de la enfermedad estudiada y cuyo análisis no es posible mediante estudios convencionales o requerirían estudios moleculares adicionales.
|
ADAMTS2 |
AEBP1 |
B3GALT6 |
B4GALT7 |
C1R |
C1S |
CHST14 |
COL12A1 |
COL1A1 |
COL1A2 |
|
COL3A1 |
COL5A1 |
COL5A2 |
DSE |
FKBP14 |
FLNA |
PLOD1 |
PRDM5 |
SLC39A13 |
TNXB |
|
ZNF469 |
ATP7A |
BGN |
EFEMP2 |
ELN |
FBN1 |
FBN2 |
LOX |
SKI |
SLC2A10 |
|
SMAD3 |
TGFB2 |
TGFB3 |
TGFBR1 |
TGFBR2 |
El panel que incluye los 21 genes prioritarios asociados con los diferentes subtipos de estos síndromes descritos hasta la fecha
|
SÍMBOLO DEL GEN |
PROTEINA |
HERENCIA* |
SED CLASIFICACIÓN |
|
ADAMTS2
|
Procolágeno I N-proteinasa (NPI))
|
AR |
SED Dermatosparaxis (dEDS) Prevalencia: <1 / 1 000 000 |
|
AEBP1 |
Proteína similar a la carboxipeptidasa aórtica (ACLP) |
AR |
Síndrome de Ehlers-Danlos clásico-like-2 Prevalencia: <1/1 000 000 |
|
B3GALT6 |
Beta-1,3-galactosyltransferase 6 también conocida como galactosiltransferasa II |
AR |
Síndrome de Ehlers-Danlos, tipo espondilodisplásico, 2. SEDsp Prevalencia: <1/1 000 000 |
|
B4GALT7 |
Beta-1,4-galactosiltransferasa 7 también conocida como galactosiltransferasa I |
AR |
Síndrome de Ehlers-Danlos, tipo espondilodisplásico, 1 Prevalencia: <1/1 000 000 |
|
Cir and CIS |
La activación intracelular de C1r y / o C1s, que puede activar la cascada clásica del complemento |
|
Las mutaciones heterocigotas de sentido erróneo o de inserción / deleción en marco en las subunidades C1r y C1s del complemento 1 causan el síndrome de Ehlers-Danlos periodontal (pEDS) |
|
CHST14 |
Dermatan-4-sulfotransferasa-1 (D4ST1) |
AR |
SED Musculocontractural (mcEDS-CHST14) Prevalencia: <1/1 000 000 |
|
COL1A1 |
colágeno alfa-1 tipo I |
AD AD AD |
-SED Clásico (cEDS) Prevalencia de 1 / 20.000 -SED Vascular (vEDS) -SED Artrocalasia (aEDS) |
|
COL1A2 |
Colágeno, tipo I, alfa 2 |
AD AR |
-SED Artrocalasia (aEDS) -SED Vascular (vEDS) |
|
COL3A1 |
Colágeno, tipo III, alfa 1 |
AD |
SED Vascular (vEDS Prevalencia 1 / 50.000 a 1 / 200.000 |
|
COL5A1 |
Colágeno, tipo V, alfa 1 |
AD |
SED Clásico (cEDS) |
|
COL5A2 |
Colágeno, tipo V, alfa 2 |
AD |
SED Clásico (cEDS) |
|
SED |
Dermatan-sulfato epimerasa (DSE) |
AR |
SED musculocontractural (mcEDS) |
|
FKBP14 |
Peptidil-prolil cis-trans isomerasa FKBP14 (Proteína 14 de unión a FK506) |
AR |
SED cifoescoliótico (kEDS-FKBP14) Prevalence 1/100,000 |
|
FLNA |
Filamina A |
XL |
SED relacionado con filamina A con heterotopía nodular periventricular La heterotopía nodular periventricular ligada al cromosoma X (XL-PH) puede presentarse principalmente con un síndrome de hipermovilidad articular. Se aconseja la detección de manifestaciones cardiovasculares a aquellos pacientes cuando existan convulsiones asociadas o un patrón de herencia ligado al cromosoma X. |
|
PLOD1 |
Procolágeno-lisina 5-dioxigenasa |
AR |
SED cifoescoliótico (kEDS - PLOD1) |
|
PRDM5 |
Proteína 5 del dedo de zinc del dominio PR (proteína 5 que contiene el dominio PR). |
AR |
Síndrome de la córnea frágil (BCS) <1 en 1,000,000, con solo alrededor de 60 casos reportados en la literatura
|
|
SLC39A13 |
Transportador de zinc ZIP13 |
AR |
SED espondilodisplásico (spEDS-SLC39A13) Prevalencia <1 / 1 000 000 |
|
TNXB |
Tenascina-X |
AR |
La mutación en el gen TNXB, que conduce a la pérdida de la proteína Tenascin X, está asociada con el desarrollo de síndromes de Ehlers-Danlos (EDS) de tipo clásico. <1 / 1 000 000; |
|
ZNF469 |
proteína de dedo de zinc 469 |
AR |
Síndrome de la córnea frágil (BCS) <1 en 1,000,000, con solo alrededor de 60 casos reportados en la literatura |
SOLAPAMIENTO (OVERLAPPING) de la presentación clínica de algunos subtipos de SED,
Actualmente existen 14 subtipos de síndromes de Ehlers-Danlos (EDS). En 13 de estos (es decir, todos excepto el subtipo hipermóvil), el diagnóstico se confirma mediante la combinación de características clínicas y la identificación de una mutación en los genes de la enfermedad correspondientes.
- Entre ellos, la clasificación actual identifica 3 subtipos de EDS que están asociados con mutaciones en los dos genes que codifican el colágeno I (denominados COL1A1 y COL1A2).
Tres de estos subtipos están asociados a mutaciones en los genes COL1A1/COL1A2:
- SED artrocalasia (SEDa), que afecta a los genes COL1A1 y COL1A2
- SED cardíaco-valvular (SEDcv) que afecta al gen COL1A2
- SED clásico relacionado con COL1A1 (SEDc-COL1A1, anteriormente denominado “SED clásico con fragilidad arterial”). Este es uno de los tipos de SED de muy baja prevalencia descriptos en forma separada en 2017.
Trastorno de solapamiento (overlapping) de osteogénesis imperfecta (OI) / Síndrome Ehlers-Danlos (SED)
que debería aplicarse a aquellas personas:
- Que presentan características múltiples del SED con o sin signos de OI leve-moderada
- Con variantes causales en los genes COL1A1 o COL1A2, pero que
- No tienen características y variantes moleculares de otros tipos de SED relacionados con estos genes. Es decir, en quienes se han descartado el SEDc-COL1A1, el SEDa y el SEDcv.
Los genes COL1A1 y COL1A2 también se asocian a la Osteogenesis Imperfecta (OI), que igual que el SED, es una Enfermedad Hereditaria del Tejido Conectivo (EHTC).
Los pacientes que mostraban características mixtas tanto de EDS como de osteogénesis imperfecta se consideraban anteriormente que tenían una superposición de ambas enfermedades.
La OI se caracteriza a grandes rasgos por un aumento de la fragilidad ósea, una baja masa ósea y una susceptibilidad a fracturas óseas de gravedad variable.
Además de los tipos de SED bien definidos y de la Osteogenesis Imperfecta, se ha reconocido que existen personas con una superposición de características entre el SED y la OI.
- Hasta ahora no estaba claro si podía considerarse un tipo de SED con defectos moleculares reconocidos (pero que se había pasado por alto al reclasificar la enfermedad),
- o si –por el contrario- no se trataba de ningún tipo de SED, y debía incluirse dentro de la clasificación de la OI.
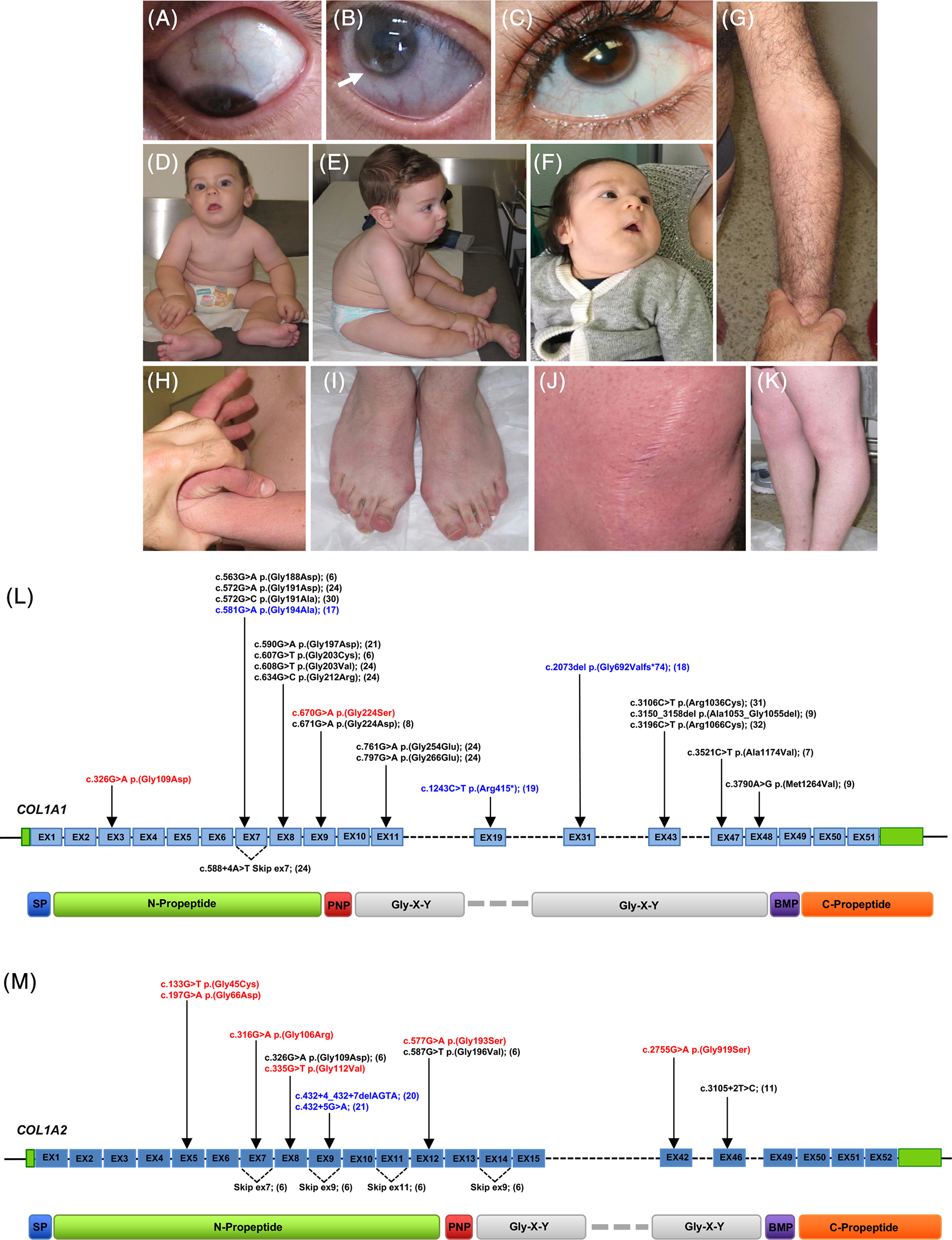
Recientemente un grupo de investigadores de diferentes países, especialistas en SED y sus enfermedades relacionadas han publicado un artículo en la revista científica Clinical Genetics, ampliando y redefiniendo el solapamiento de osteogénesis imperfecta OI/SED como un tipo de SED ausente en la clasificación de 2017.
Los investigadores registraron las características, signos y síntomas de 21 personas de 13 familias, en las que encontraron variantes en los genes COL1A1/COL1A2 después de sospechar que tenían SED. Ninguna de estas personas pudo clasificarse como afectada, ni por OI, ni por cualquiera de los tres tipos de SED reconocidos hasta ahora asociados con los genes COL1A1/COL1A2.
- SED artrocalasia (SEDa), que afecta a los genes COL1A1 y COL1A2
- SED cardíaco-valvular (SEDcv) que afecta al gen COL1A2
- SED clásico relacionado con COL1A1 (SEDc-COL1A1, anteriormente denominado “SED clásico con fragilidad arterial”). Este es uno de los tipos de SED de muy baja prevalencia descriptos en forma separada en 2017.
Sugiriendo la denominación de Trastorno de superposición de osteogénesis imperfecta / SED
En su opinión, este subgrupo de pacientes con SED debe separarse de la OI (osteogénesis imperfecta clásica ) al menos por la afectación multisistémica, y puede ser clínica y molecularmente distinguible de las otras variantes de SED.
CONCLUSIONES
1. Existe una superposición o solapamiento (en inglés overlapping) de síntomas entre los subtipos de SED. Entre ellos, la clasificación actual identifica 3 subtipos de SED que están asociados con mutaciones en los dos genes que codifican el colágeno I (denominados COL1A1 y COL1A2): SED artrocalasia (SEDa), que afecta a los genes COL1A1 y COL1A2; SED cardíaco-valvular (SEDcv) que afecta al gen COL1A2 y SED clásico relacionado con COL1A1 (SEDc-COL1A1), anteriormente denominado “SED clásico con fragilidad arterial”
2. Solapamiento con otros trastornos del tejido conectivo: Trastorno de solapamiento (overlapping) de osteogénesis imperfecta (OI) / Síndrome Ehlers-Danlos (SED).
REFERENCIA
- Morlino S, et al. COL1-related overlap disorder: A novel connective tissue disorder incorporating the osteogenesis imperfecta/Ehlers-Danlos syndrome overlap. Clin Genet 2020 ;97:396-406.
PROF. DR. FERNANDO GALAN