Fernando Galán Galán
Profesor Titular de Medicina
Especialista en Medicina Interna
Experto en Miopatía Mitocondrial del Adulto
Fibromialgía y Síndrome de Fatiga crónica
BLOG
LA NUEVA TÉCNICA CRISPR LLAMADA EDICIÓN PRINCIPAL (PRIME EDITING) 2019
La nueva técnica, llamada edición principal (Prime editing), está diseñada para superar algunas de las limitaciones de CRISPR.
Pero sigue siendo solo una prueba de laboratorio, no una técnica terapéutica.
A pesar de la facilidad con la que la popular herramienta de edición de genes CRISPR-Cas9 altera los genomas, todavía es algo propensa a errores y efectos no deseados.
El método alternativo, llamado edición principal, mejora las posibilidades que los investigadores realicen solamente las ediciones que desean, en lugar de una combinación de cambios que no pueden predecir.
CRISPR-Cas9 y la edición principal funcionan cortando el ADN en un punto específico del genoma.
- CRISPR-Cas9 rompe ambas cadenas de la doble hélice de ADN y luego se basa en el propio sistema de reparación de la célula para reparar el daño y realizar las ediciones. Pero ese sistema de reparación no es del todo fiable y puede conducir a una mezcla incontrolable de ediciones que varían entre las células.
- Además, incluso cuando los investigadores incluyen una plantilla para guiar cómo se edita el genoma, el sistema de reparación de ADN en la mayoría de las células es mucho más probable que realice esas pequeñas inserciones o deleciones aleatorias, que agregar una secuencia de ADN específica al genoma. Eso hace que sea difícil, y en algunos casos, casi imposible, que los investigadores usen CRISPR-Cas9 para agregar una secuencia de ADN con una secuencia de su elección.
La edición principal evita estos problemas.
- Aunque también utiliza Cas9 para reconocer secuencias de ADN específicas, al igual que CRISPR-Cas9, la enzima Cas9 en la herramienta de edición principal se modifica para cortar una sola hebra de ADN.
- Luego, una segunda enzima llamada transcriptasa inversa y guiada por una cadena de ARN, realiza las ediciones en el sitio del corte.
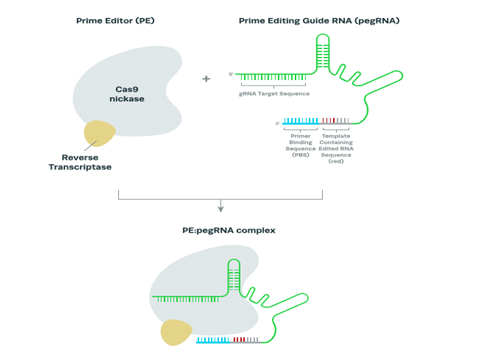
Un complejo de edición principal (PE) está compuesto por:
- Cas9 nickase y Transcriptasa inversa
- Guía de edición principal ARN (pegRNA):
- Una guía con ARN de la secuencia diana (gRNA), 5´
- Una guía ARN con Secuencias de unión a 3´ primer,
- Plantilla que contiene secuencia de ARN editada
Cas9 nickase: es una forma mutante de la nucleasa Cas9 donde uno de sus dominios de escisión ha sido desactivado.
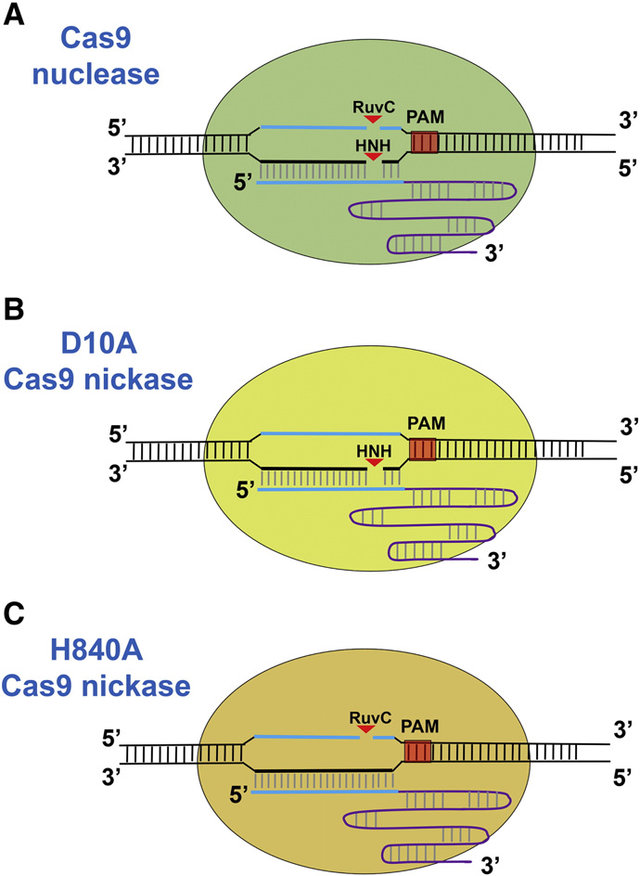
(A) La nucleasa Cas9 de tipo salvaje genera roturas bicatenarias en los sitios diana de ADN con complementariedad al extremo 5 'de un ARNg. Los dos dominios de nucleasa efectivos son los dominios RuvC y HNH (puntas de flecha rojas).
(B) D10A Cas9 nickase es creada por una mutación puntual D10A en el dominio de la nucleasa RuvC. D10A Cas9 nickase escinde específicamente la cadena de ADN complementaria a gRNA.
(C) H840A Cas9 nickase es creada por una mutación puntual H840A en el dominio de nucleasa HNH. La H840A Cas9 nickase escinde la cadena de ADN no complementaria a gRNA.
Prime editing consta de tres elementos
- una enzima ampliamente utilizada en el sistema CRISPR clásico: Cas9. Cas9 nickcase, nucleasa modificada para cortar únicamente una de las dos cadenas de ADN, en lugar de introducir un corte limpio que deje dos extremos libres en la hebra de ADN, como hace en el sistema CRISPR.
- una transcriptasa inversa o reversa, una enzima que se caracteriza por generar una secuencia de ADN utilizando como molde ARN.
- un fragmento de ARN, denominado pegRNA (de prime editing guide RNA), que tiene dos funciones:
- Por una parte pegRNA situa a Cas9 nickcase en una posición concreta del ADN.
- Por otra, actúa como molde para la síntesis de ADN por la transcriptasa reversa.
Es decir, el pegRNA incluye la información con el cambio que se desea realizar en el genoma.
Si alguno de esos tres eventos de emparejamiento de ADN falla, entonces la edición principal no puede continuar.
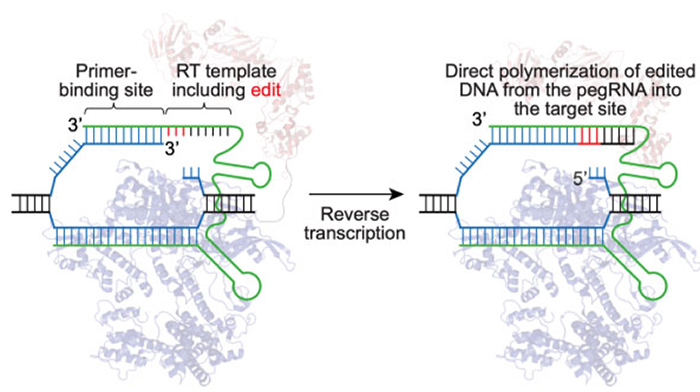
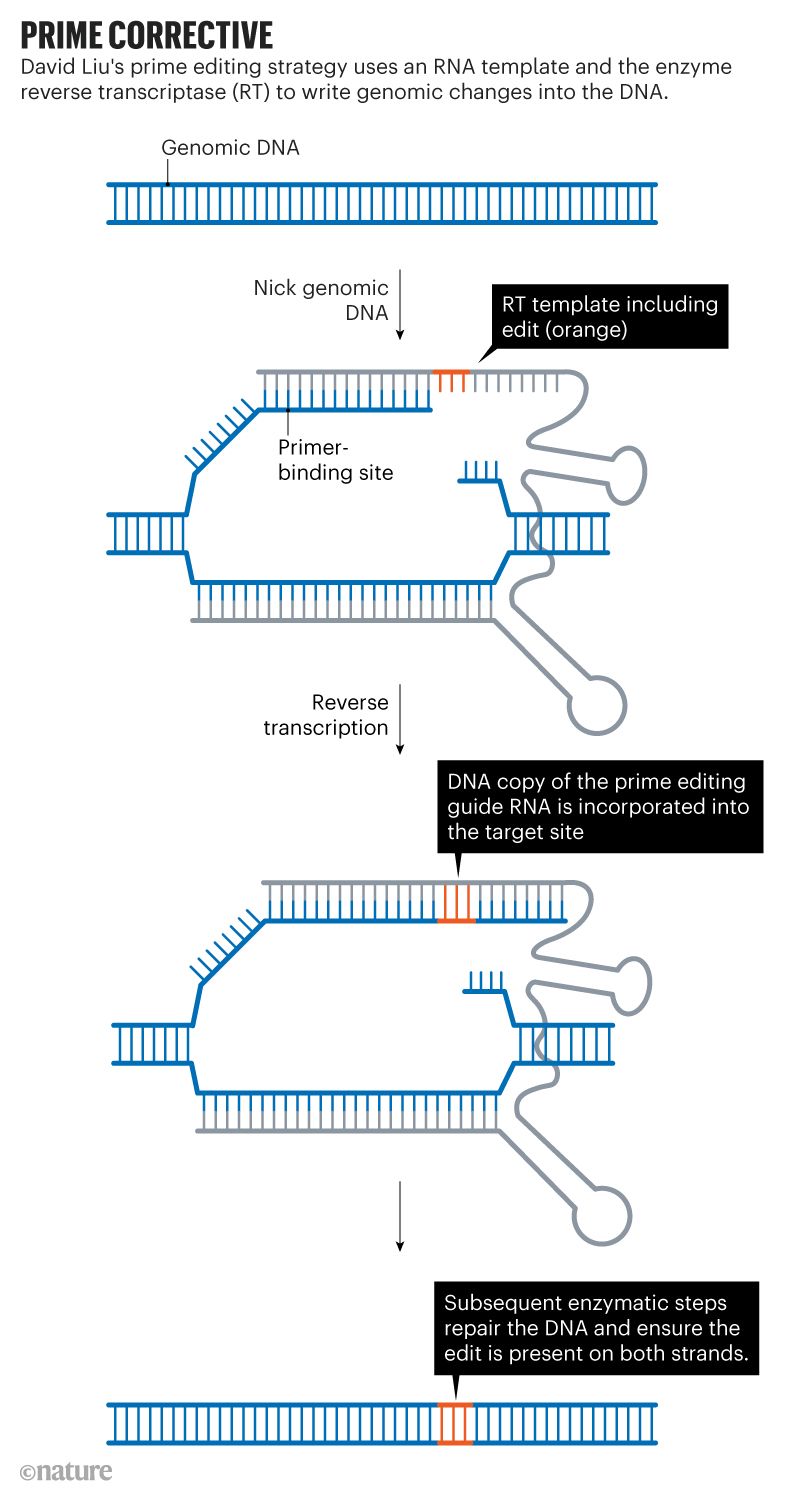
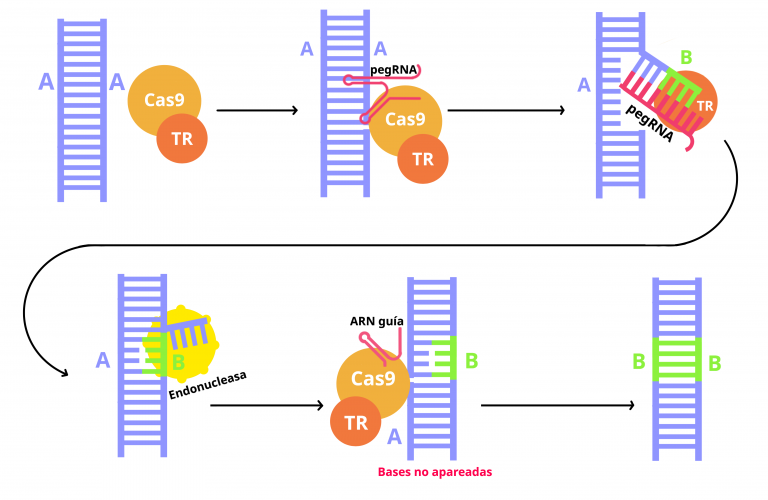
- En un primer paso el pegRNA (en rojo), que forma un complejo con Cas9 y la transcriptasa reversa, se une por uno de sus extremos a una región específica del genoma por complementariedad de secuencia.
- Una vez posicionada, la nucleasa Cas9 introduce un corte en solo una cadena de ADN que es aprovechado por la transcriptasa reversa, que utiliza el otro extremo del propio pegRNA como molde para sintetizar ADN (en verde la nueva cadena).
- El fragmento original de ADN que queda expuesto tras sintetizar la nueva cadena es eliminado por endonucleasas propias de la célula, de forma que el resultado de esta primera etapa es una molécula de ADN con una posición desapareada entre sus cadenas, ya que una hebra es la original y la otra tiene una modificación.
- Para resolver esta situación, en una segunda etapa se utiliza un ARN guía que dirige de nuevo a la enzima Cas 9 a la cadena del ADN no modificada. Cas9 introduce un corte en esta cadena que alerta a los mecanismos de reparación de la célula, que utilizarán la cadena modificada como molde para reparar el ADN
Un editor de documentos de un ordenador personal es realmente la imagen correcta, si desea imaginar cómo funciona la nueva molécula de ingeniería Prime editing de Liu.
- Primero, los investigadores agregan un poco de texto genético que quieren poner en un genoma (piense en eso como el comando "copiar"). Cas9 entonces actúa como el cursor, encontrando la posición correcta en el ADN.
- Por último, la transcriptasa inversa actúa como un comando de "pegar", copiando el texto genético preparado por los científicos.
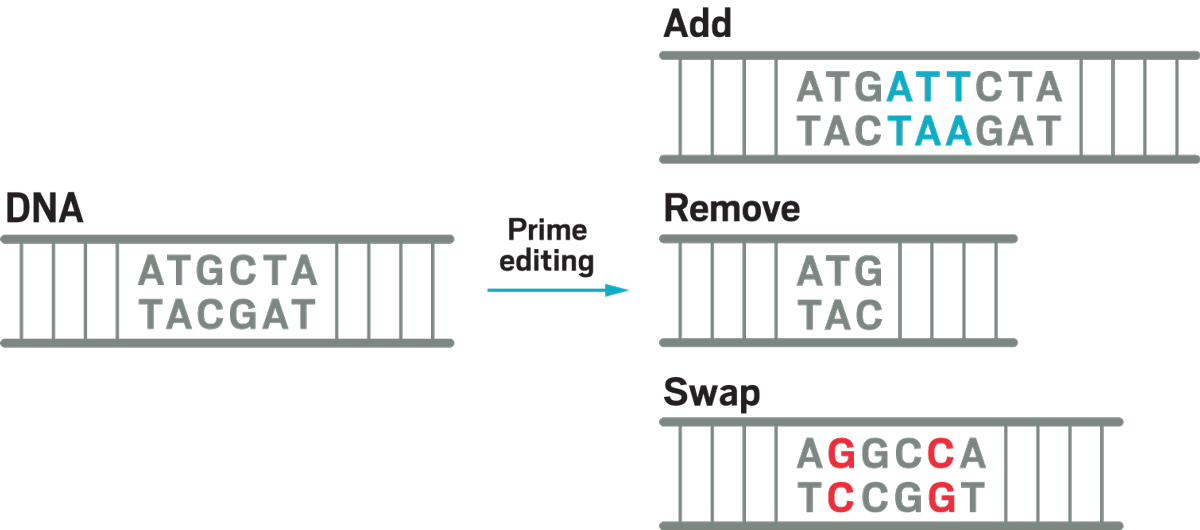
Los nuevos editores principales de CRISPR pueden agregar o eliminar tramos cortos de ADN o cambiar cualquier letra por otra. Ejemplos de la edición principal:
- agrega una secuencia ATT al ADN,
- elimina una secuencia de CTA
- y cambia un par de bases T: A por un par G: C y otro par de bases T: A para un par C: G.
Sin embargo, la edición principal tiene limitaciones.
- Primero, la danza molecular sofisticada de múltiples pasos que ocurre entre los componentes de edición principal aún no es predecible y no siempre resulta como se esperaba. Por lo tanto, aún pueden surgir ediciones aleatorias imperfectas, lo que significa que es posible que sea necesario probar varias combinaciones de componentes para resolver las coreografías requeridas para cada edición de interés.
- En segundo lugar, introducir el gran sistema de edición principal en algunos tipos de células podría ser un desafío, dado que muchos intentos anteriores han fallado con el sistema CRISPR/Cas9 convencional, que es aproximadamente la mitad del tamaño.
Para fines de investigación, estas limitaciones son en su mayoría simplemente inconvenientes, y probablemente se superarán mediante un trabajo de seguimiento dirigido a una mejor comprensión y ajuste del método.
Sin embargo, para aplicaciones médicas, estos problemas presentan un desafío mucho mayor: las ediciones imperfectas de ADN son inaceptables, y la entrega eficiente del sistema de edición principal a las células será crucial. Entonces, aunque la edición principal ciertamente tiene el potencial de darnos un control sin precedentes, solo el tiempo dirá si se convierte en una herramienta más en la caja de herramientas CRISPR o una cura para todas las enfermedades genéticas.
CONCLUSIONES
- Un complejo de edición principal (PE) está compuesto 3 elementos por: Cas9 nickase; transcriptasa inversa; y un fragmento de ARN, denominado pegRNA (de prime editing guide RNA (Guía de edición principal ARN (pegRNA)
- La primera limitación es la danza molecular sofisticada de múltiples pasos que ocurre entre los componentes de edición principal aún no es predecible y no siempre resulta como se esperaba.
- La segunda limitación es el tamaño del sistema de edición principal, doble que el sistema CRISPR/Cas9 convencional
- Para fines de investigación, estas limitaciones son en su mayoría simplemente inconvenientes
- Para aplicaciones médicas, estos problemas presentan un desafío mucho mayor: las ediciones imperfectas de ADN son inaceptables, y la entrega eficiente del sistema de edición principal a las células será crucial.
- Sigue siendo solo una prueba de laboratorio, no una técnica terapéutica
REFERENCIA
Anzalone AV, Randolph PB, Davis JR, Sousa AA, Koblan LW, Levy JM, Chen PJ, Wilson C, Newby GA, Raguram A, Liu DR. Search-and-replace genome editing without double-strand breaks or donor DNA. Nature. 2019;576:149-157. doi: 10.1038/s41586-019-1711-4.
PROF. DR. FERNANDO GALAN




